
11
DENK(T)RÄUME Mobilität
Band 5: Chemie und Sport
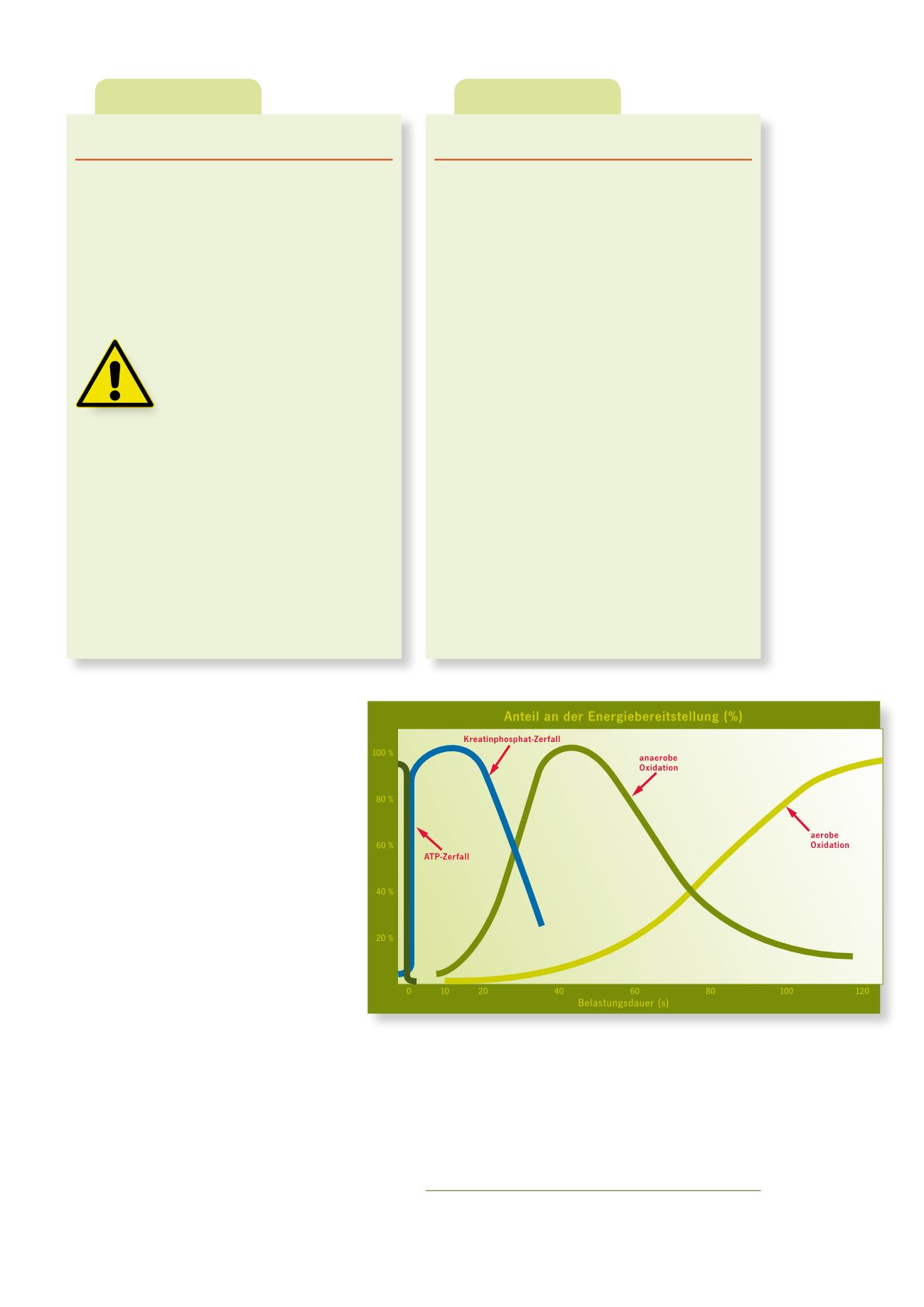
Abb. 1: Zeitlicher
Verlauf der Energie-
bereitstellung bei
sportlicher Aktivität.
Nach: P. Markworth:
Sportmedizin. Phy-
siologische Grundla-
gen. rororo, Reinbeck
2000, S. 256
von Adenosintriphoshat mit Wasser zu Adeno-
sindiphosphat und Phosphat liefert –30,5 kJ/
mol, die von Adenosintriphosphat mit Wasser
zu Adenosinmonophosphat und Diphosphat
–32,5 kJ/mol. Diphosphat hydrolysiert weiter
zu zwei Molekülen Phosphat, verbunden mit
einer freien Enthalpie von –33,5 kJ/mol. Es
können also insgesamt zwei sehr energiereiche
Phosphorsäureanhydrid-Bindungen konsu-
miert werden. Die viel weniger exergonische
Hydrolyse der ortho-glykosidischen P-O-C-
Einheit im Adenosinmonophosphat zu Ade-
nosin und Phosphat (ca. –9 kJ/mol) spielt bei
der Energieversorgung der Muskeln praktisch
keine Rolle.
Wenn man einen Löffel des Säureanhydrids
Phopshor(V)-oxid in ein Becherglas mit Wasser gibt,
bildet sich unter heftigem Zischen und Erwärmen
Phosphorsäure – ein geeignetes Experiment (Versuch
2: Hydrolyse von Phosphor(V)-oxid), um Schülern
ergänzend die Energie zu verdeutlichen, die in dem
P-O-P-Strukturelement steckt.
Bei Schnellkraftsportarten (Speerwurf, Weitsprung,
Sprints etc.) muss die ATP-Bereitstellung rasch ge-
schehen. Der ATP-Nachschub erfolgt deshalb fast
ausschließlich anaerob, wobei als Abbauprodukt der
Glucose u. a. Milchsäure entsteht. Die damit verbun-
dene Senkung des pH-Wertes bewirkt, dass der Mus-
kel steifer und weniger leistungsfähig wird. (Eine wei-
tere Ursache für den Muskelkater sind kleinste Ver-
letzungen auf der Zellebene der elastischen bindege-
webigen Muskelbestandteile
3
.)
3
D. Voet, J. G. Voet, C. W. Pratt:
Fundamentals of Biochemistry. Wiley, New
York 1999, S. 362
INFO-BOX
Versuch 1
Zucker-Verbrennung in einer Kaliumchlorat-
Schmelze
Geräte
Stativ, schwer schmelzbares großes (200 x 30 mm)
Reagenzglas
Chemikalien
Kaliumchlorat (O, brandfördernd), Würfelzucker
Sicherheitshinweis
Der Versuch muss hinter einer Schutz-
scheibe unter dem Abzug oder im Freien
durchgeführt werden.
Durchführung
1-2 g Kaliumchlorat werden im Reagenzglas über dem
Brenner geschmolzen. In die Schmelze wirft man ein
kleines (!) Stück Würfelzucker.
Vorsicht:
Bei der Reaktion kann Kaliumchlorat von dem
entstehenden Kohlendioxid und Wasser mitgerissen und
aus dem Reagenzglas geschleudert werden.
Beobachtung
Das Gummibärchen verbrennt unter intensivem Auf-
glühen, „tanzt“ auf der Salzschmelze und erzeugt ein
pfeifendes Geräusch.
INFO-BOX
Versuch 2
Hydrolyse von Phosphor(V)-oxid
Geräte
Becherglas (500 ml, hohe Form), Spatel, Glasstab,
Thermometer
Chemikalien
Phosphor(V)-oxid (C, ätzend), Universalindikator-Lösung
Durchführung
Ein Becherglas wird etwa zu einem Viertel mit Leitungs-
wasser gefüllt, dem tropfenweise Universalindikator bis
zur kräftigen Färbung zugesetzt wird.
Die Temperatur wird gemessen. Anschließend wird eine
reichliche Spatelspitze Phosphor(V)-oxid zugeben. Nach
dem Abklingen der Reaktion wird mit dem Glasstab um-
gerührt und erneut die Temperatur gemessen.
Beobachtung
Bei Zugabe von ca. 3 g Phosphor(V)-oxid zu 120 ml
Wasser erhitzt sich die Lösung erkennbar (T
(vorher)
=
21°C; T
(nachher)
= 26°C). Der aufsteigende Wasserdampf
reißt Phosphor(V)-oxid mit. Verbunden mit einem
zischenden Geräusch bildet sich weißer Rauch. Der
Universalindikator wird rot.


















